Définition
Qu’est-ce que c’est ?
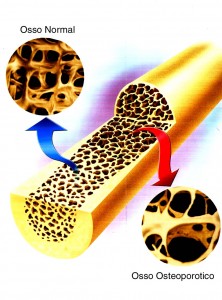
L’ostéoporose devient un véritable fléau mondial. L’allongement actuel de la durée de vie (on gagne trois mois d’espérance de vie par année de vie) en fait une des nécessités médicales et socio-économiques du 21e siècle. Actuellement, parmi 100 femmes atteignant l’âge de la ménopause, 40 seront victimes, avant la fin de leur vie, d’une fracture ostéoporotique : fracture du poignet, tassement vertébral, fracture du col du fémur.
Entre 4 et 7 milliards de francs
Chaque année en France, on recense 35 000 nouvelles fractures du poignet, 60 000 nouveaux tassements vertébraux et 50 000 nouvelles fractures de l’extrémité supérieure du fémur. Le coût médical des fractures liées à l’ostéoporose serait évalué actuellement en France entre 4 et 7 milliards de francs par an.
En 2050, il est prévu un triplement des fractures de l’extrémité supérieure du fémur, avec leurs conséquences : augmentation de la mortalité dans l’année qui suit la fracture, dégradation de la qualité de vie, coûts socio-économiques (chirurgie, hospitalisation…).
Une des priorités de l’organisation mondiale de la santé
L’Organisation mondiale de la santé (OMS) a fait de la prévention et de la prise en charge de l’ostéoporose un de ses objectifs prioritaires lors de la Journée mondiale de l’ostéoporose (20 octobre 1999). Elle a établi un programme international d’éducation, visant à améliorer le diagnostic et le traitement de l’ostéoporose :
- le diagnostic doit pouvoir être effectué avant la fracture, grâce à l’analyse clinique des facteurs de risque, et surtout grâce à la mesure de la densité osseuse, par la densitométrie osseuse ;
- le traitement doit être préventif, à tous les âges de la vie.
Symptômes
Quels examens ?
Le diagnostic de l’ostéoporose est actuellement possible avant le stade de la fracture, et prend tout son intérêt dans la mesure où il débouche sur des mesures thérapeutiques. Il est fait par la mesure de la densité osseuse ou densitométrie osseuse.
De nombreuses études ont permis de conclure que 75 à 80 % de la résistance d’un tissu osseux s’expliquent par la densité osseuse. Plusieurs études prospectives ont mis en évidence une relation étroite entre la diminution de la densité minérale osseuse (DMO) et le risque de fracture : le risque fracturaire est doublé pour chaque diminution de la DMO d’une déviation-standard. La mesure de la DMO va donc permettre de faire le diagnostic d’ostéoporose, et d’évaluer le risque des complications de la maladie liées aux fractures.
Les méthodes de mesure reposent sur l’atténuation de l’énergie d’un faisceau de photons ou d’ultrasons. La radiographie conventionnelle ne permet pas de faire de diagnostic d’ostéoporose. L’absorptiométrie biophotonique à rayons X (DEXA aux Etats-Unis) représente la référence actuelle. Sa précision et sa reproductibilité permettent de faire un diagnostic fiable et de suivre l’évolution. L’irradiation est faible.
La mesure de la densité osseuse par ultrasons permet, comme l’absorptiométrie biphotonique, d’évaluer le risque fracturaire, mais elle ne permet pas actuellement de suivre l’évolution de l’ostéoporose ou de ses traitements.
Les modalités de l’examen
Les deux sites explorés sont le rachis lombaire et l’extrémité supérieure du fémur. Pour le rachis lombaire, les vertèbres examinées sont L1 à L4 ou L2 à L4. La mesure peut être faussée par une arthrose importante : elle est donc moins intéressante au-delà de 50 ans. On peut analyser différentes régions de l’extrémité supérieure du fémur : le col est intéressant pour le diagnostic mais, pour suivre l’évolution, il est préférable de s’intéresser à la valeur totale.
Le Z score est la mesure de l’écart entre la valeur du patient et la valeur moyenne des sujets normaux de même âge et de même sexe : 95 % des valeurs de la population se situent entre Z+2 et Z-2. Le T score est la mesure de l’écart entre la valeur du patient et la valeur moyenne des adultes jeunes (20-30 ans) de même sexe.
L’OMS a établi une nouvelle définition de l’ostéoporose fondée sur la mesure du T score par la densitométrie osseuse :
- DMO normale : T score supérieur à -1 ;
- ostéopénie : T score compris entre -2,5 et -1 ;
- ostéoporose : T score inférieur à -2,5 ;
- ostéoporose confirmée : le T score est inférieur à -2,5 et il existe au moins une fracture ostéoporotique.
Malheureusement, cette définition exige une standardisation parfaite des appareils, ce qui n’est pas le cas actuellement.
Les indications de la densitométrie osseuse
La densitométrie n’est utile à la ménopause que si son résultat influence la décision thérapeutique. Pour beaucoup, son indication se discute plutôt vers 60-65 ans : la découverte d’une ostéoporose déclenchera la prise en charge thérapeutique. Elle est indispensable en cas de fracture suspectée d’être ostéoporotique, pour affirmer le diagnostic d’ostéoporose avant le traitement.
On peut être conduit à faire une densitométrie en cas d’anomalie radiologique : apparence de déminéralisation, déformation vertébrale isolée. Lorsque l’on envisage une corticothérapie prolongée, il est intéressant de faire une densitométrie osseuse de départ, et d’adjoindre à la corticothérapie un traitement préventif de l’ostéoporose cortisonique.
Lors de la surveillance des traitements de l’ostéoporose, il est tentant de suivre l’évolution densitométrique : compte tenu des contraintes de la technique et de la faible variation de la densité osseuse sous traitement, un délai de 18 mois à 2 ans est nécessaire entre deux mesures.
Il est important de faire une densitométrie en cas d’arrêt d’un traitement d’ostéoporose quel qu’il soit, pour avoir une référence à l’arrêt.
Certains examens biologiques sont indispensables lorsque l’on découvre une ostéoporose, pour éliminer une ostéoporose secondaire. D’autres sont de connaissance plus récente, mais extrêmement intéressants pour l’évaluation du risque fracturaire et l’évolution sous traitement.
Les examens biologiques standards
Un certain nombre d’examens biologiques sont indispensables lorsque l’on découvre une ostéoporose, essentiellement pour rechercher une cause autre que la ménopause.
Il faut faire une prise de sang qui permettra le dosage du calcium, du phosphore, de la créatinine (reflet de la fonction rénale) et des protides (la calcémie, teneur en calcium, n’a de valeur que ramenée à la protidémie, teneur en protides), ainsi que la réalisation d’une numération des éléments sanguins. Il faut faire un recueil des urines de 24 heures, permettant de doser le calcium et la créatinine.
D’autres examens peuvent être faits selon le contexte clinique et le résultat des premiers examens biologiques : dosages hormonaux (hormones thyroïdiennes, parathormone, cortisol, testostérone chez l’homme), bilan hépatique.
La mesure des marqueurs biochimiques du remodelage osseux
Ils sont de connaissance récente. Ce sont les constituants de la matrice osseuse, libérés pendant la formation ou la destruction osseuse :
- pour la formation osseuse, ostéocalcine, dosée dans le sang ;
- pour la destruction osseuse, déoxypyridinoline, peptides du collagène (NTX, CTX), dosés dans les urines.
Leur dosage a un premier intérêt : une résorption osseuse anormalement élevée, définie par une augmentation des taux de pyridinoline ou de peptides (CTX, NTX) par rapport aux valeurs observées chez les femmes non ménopausées, est associée à un doublement du risque de fracture de l’extrémité supérieure du fémur chez la femme âgée. Ce facteur de risque est indépendant de la densité minérale osseuse (DMO), mesurée par densitométrie osseuse.
Ainsi, une femme ayant une DMO basse (T score inférieur à -2,5) et un taux de pyridinoline élevé, aura un risque de fracture de l’extrémité supérieure du fémur 4 à 5 fois plus élevé que celui des femmes à DMO et pyridinoline normale. L’association de ces deux mesures (DMO et pyridinoline) permettra donc d’identifier les femmes à très haut risque de fracture.
Par ailleurs, sous l’effet des traitements, les marqueurs du remodelage osseux chutent rapidement en 3 à 6 mois. Cette diminution est corrélée au gain osseux mesuré à la densitométrie après 18 mois à 2 ans. La mesure de l’évolution des marqueurs du remodelage du traitement permet donc également de juger plus rapidement de l’efficacité de celui-ci.
D’où cela vient-il ?
Il faut distinguer les ostéoporoses dites « primitives », les plus fréquentes, et les ostéoporoses « secondaires ».
Les ostéoporoses primitives
Elles sont divisées en sous-groupes, selon l’âge de survenue :
- L’ostéoporose juvénile, avant 25 ans, est exceptionnelle.
- L’ostéoporose du sujet jeune est rare : elle touche plus l’homme que la femme. Les facteurs génétiques jouent un rôle important.
- L’ostéoporose de la grossesse : la grossesse et l’allaitement favorisent une perte osseuse modérée, qui est récupérée dans les 6 mois après l’arrêt de l’allaitement.
- L’ostéoporose de la ménopause : ménopause naturelle ou chirurgicale, absence prolongée de règles.
- L’ostéoporose du vieillissement concerne les hommes et les femmes après 70 ans.
- Les causes héréditaires sont rares : c’est l’ostéogenèse imparfaite ou maladie de Lobstein (ou maladie des sclérotiques bleues).
Les ostéoporoses secondaires
Elles sont nombreuses :
- Traitement prolongé par la cortisone (plus de 6 mois) à dose forte (supérieure à 7,5 mg/j).
- Maladies endocriniennes : insuffisance en hormones sexuelles, d’origine hypophysaire ou gonadique ; hyperfonctionnement de la thyroïde ou d’une parathyroïde ; hyperfonctionnement de la corticosurrénale (maladie de Cushing) ; diabète.
- Rhumatismes inflammatoires : polyarthrite rhumatoïde surtout, mais aussi spondylarthrite ankylosante ou arthrite chronique juvénile.
- Maladies digestives : maladies chroniques de l’intestin ; insuffisance hépatique.
- Maladies rares : hémochromatose, mastocytose.
- Autres causes : immobilisation prolongée ; malnutrition sévère, anorexie mentale ; intoxication alcoolo-tabagique ; insuffisance rénale ; fuite rénale chronique de calcium.
Plusieurs causes peuvent s’associer pour favoriser la survenue d’une ostéoporose.
Comment cela marche-t-il ?
L’os est un tissu en renouvellement permanent. Selon les périodes de la vie, c’est la formation ou la destruction qui va prédominer.
L’os est un tissu vivant qui se renouvelle en permanence grâce au fonctionnement couplé de deux sortes de cellules :
- les ostéoclastes détruisent l’os ancien : c’est la résorption osseuse ;
- les ostéoblastes fabriquent l’os nouveau : c’est la formation osseuse.
Il existe en principe un équilibre entre destruction et formation osseuse, sous l’influence de nombreux facteurs (vitamine D, hormones sexuelles, parathormone, hormones thyroïdiennes, cortisol…). Après 30 ans, le vieillissement de l’os se traduit par une perte osseuse due à un déséquilibre en faveur de la résorption osseuse. Par ailleurs, un dérèglement du remodelage osseux peut être la cause de nombreuses maladies de l’os.
L’évolution de la masse osseuse est schématiquement divisée en trois périodes.
La phase de croissance rapide
Elle se situe de la naissance à la fin de la deuxième décennie (18-20 ans) : elle permet l’établissement de la masse osseuse maximale, capital osseux de base ou pic de masse osseuse.
Au moment de la puberté, une différence de masse osseuse entre les sexes s’instaure : elle est due essentiellement à une croissance plus prolongée de cette masse osseuse chez le garçon, avec un accroissement plus important de la taille des os. Le gain de masse osseuse se fait entre 11 et 14 ans chez la fille et diminue après 16 ans. Il se fait chez le garçon de 13 à 17 ans et se poursuit de 17 à 20 ans.
De nombreux facteurs interviennent sur le gain de la masse osseuse pendant la croissance :
- facteurs génétiques, probablement les plus importants ;
- facteurs mécaniques : activité physique, poids corporel ;
- facteurs nutritionnels : apport calorique global, apport protéique, apport calcique ;
- facteurs toxiques : alcool, tabac.
La phase en plateau
Elle dure une dizaine d’années : le tissu osseux est renouvelé de façon continue par un processus de remodelage osseux. Il y a en permanence un équilibre entre destruction et formation osseuse, contribuant au maintien de la masse osseuse.
La phase de perte osseuse physiologique
Elle commence une fois la maturité osseuse atteinte et se poursuit jusqu’à la mort : ce phénomène se traduit différemment chez l’homme et chez la femme.
Chez l’homme, la perte osseuse est lente, régulière et linéaire : 0,5 à 1 % par an.
Chez la femme, elle s’accélère à la ménopause : 3 à 5 % par an pendant deux à trois ans, puis 1 à 2 % par an dans les cinq à dix ans suivant la ménopause. On parle de perte osseuse rapide post-ménopausique : elle est due à une augmentation de la destruction osseuse liée au déficit en œstrogènes. La diminution de la masse osseuse se stabilise ensuite autour de 0,5 à 1 % par an.
Chez les personnes âgées de plus de 70 ans, la perte osseuse ne s’arrête pas. Elle est aggravée par la carence en calcium et en vitamine D.
L’ostéoporose peut donc survenir lorsque le capital osseux de départ est trop bas ou la perte osseuse trop rapide.
Quels risques ?
Il existe un certain nombre de facteurs de risques qui peuvent favoriser une accélération de la perte osseuse. Ils permettent le dépistage des sujets à risques et un traitement plus précoce.
Les facteurs génétiques
Certains facteurs génétiques et constitutionnels peuvent favoriser la survenue d’une ostéoporose. Celle-ci est plus fréquente chez les sujets à peau blanche et les Asiatiques que chez les sujets à peau noire, chez les femmes petites et maigres ou en cas d’antécédents familiaux d’ostéoporose de fracture ostéoporotique. Ce sont malheureusement des facteurs contre lesquels on ne peut pas lutter.
Les autres facteurs
D’autres facteurs peuvent éventuellement être combattus.
La carence en hormones sexuelles féminines favorise l’ostéoporose. Il faut donc dépister :
- une puberté tardive ;
- des troubles des règles prolongés (en particulier dans l’anorexie mentale ou chez les sportifs de haut niveau) ;
- une ménopause précoce (avant 40 ans), naturelle ou chirurgicale (ablation des ovaires).
Des facteurs nutritionnels et environnementaux peuvent intervenir :
- Un régime pauvre en produits laitiers peut être responsable d’une carence en calcium, surtout chez l’enfant et la personne âgée. Chez l’adulte, attention aux régimes amaigrissants qui ont tendance à supprimer les produits laitiers !
- Une carence en vitamine D peut survenir en raison d’un ensoleillement insuffisant : la vitamine D est fabriquée par la peau sous l’action des ultraviolets du soleil. Cette carence peut concerner les personnes âgées qui sortent peu.
- L’excès alimentaire de sel ou de protéines animales (viande, poisson, œufs) peut favoriser la fuite de calcium dans les urines.
- Le tabac, l’alcool et le café sont reconnus comme préjudiciables pour l’os.
L’ activité physique est importante : l’absence d’activité physique ou une immobilisation prolongée sont des facteurs de risque d’ostéoporose.
Certains médicaments peuvent favoriser la survenue de l’ostéoporose : corticoïdes, hormones thyroïdiennes à visée suppressive, héparine (si le traitement est de longue durée).
Comment vivre avec ?
L’étude des facteurs de risques d’ostéoporose met en relief l’importance des facteurs nutritionnels et environnementaux : il faut donc être vigilant en ce qui concerne l’hygiène de vie.
L’alimentation
Elle doit être riche en calcium, car celui-ci joue un rôle important dans l’acquisition et le maintien de la masse osseuse.
Une conférence de consensus, réunie aux USA en 1994, a fixé les apports conseillés en calcium selon l’âge :
- chez l’enfant de moins de 5 ans : 800 mg par jour ;
- chez l’enfant de 5 ans à la puberté : 800 à 1 200 mg par jour ;
- chez l’adolescent et l’adulte jeune : 1 200 à 1 500 mg par jour ;
- chez l’homme : 1 000 mg/j de 25 à 65 ans ; 1 500 mg/j après 65 ans ;
- chez la femme : 1 000 mg/j de 25 à 50 ans ; 1500 mg/j en cas de grossesse et d’allaitement ; 1 500 mg/j après la ménopause, ou 1 000 mg/j en cas de traitement hormonal substitutif.
Le calcium ne fait pas grossir. En revanche, certains aliments riches en calcium sont caloriques (fromages…) : il faut sélectionner les produits laitiers les moins caloriques. Le lait de soja est plus pauvre en calcium que le lait de vache. Il doit donc être enrichi en calcium.
Il faut éviter l’excès de sel et de protéines animales (viandes, poissons, œufs) qui augmentent la fuite de calcium dans les urines. Le tabac, l’alcool et le café sont néfastes pour l’os.
Les aliments contenant de la vitamine D sont peu nombreux : huile de foie de morue, poissons gras, jaune d’œuf. Il ne faut donc pas compter sur l’alimentation pour combler une carence en vitamine D.
L’exposition solaire assure la production de vitamine D
La vitamine D est fabriquée par la peau sous l’effet des rayons ultraviolets ; elle est ensuite transformée par le foie et par les reins pour assurer ses fonctions. Il faut donc une exposition solaire suffisante pour ne pas manquer de vitamine D : une heure par jour, tête et bras nu, est suffisante.
C’est en hiver et dans les zones urbaines que les taux de vitamine D sont les plus bas. Une activité extérieure normale dans les mois d’été suffit le plus souvent à éviter une carence. L’excès de protection (chapeau, manches longues) peut être une cause de carence en vitamine D, de même qu’un écran total appliqué de façon efficace.
L’activité physique est un élément important de la prévention de l’ostéoporose
De même qu’un vase fragile ne se casse que s’il tombe, une fracture ostéoporotique ne survient sur un os fragile qu’en cas de chute.
L’exercice physique augmente l’activité des cellules osseuses et entretient la solidité de l’os, mais aussi améliore la force, la souplesse, l’équilibre et diminue le risque de chute. Il faut donc faire un exercice physique régulier, en évitant les activités qui peuvent faire tomber ou qui entraînent des contraintes trop importantes (port de charges).
Quel traitement ?
Dans la mesure où le dépistage de l’ostéoporose est de plus en plus précoce et performant, la prise en charge thérapeutique de l’ostéoporose doit mettre l’accent sur la prévention.
Le traitement hormonal substitutif (THS) est la base de la prévention de l’ostéoporose chez la femme ménopausée.
Le traitement hormonal substitutif
Les œstrogènes diminuent la résorption osseuse. De nombreuses études ont montré l’effet bénéfique de l’administration d’œstrogènes sur la densité osseuse, ainsi que sur la réduction du risque fracturaire. L’adjonction de progestatifs ne réduit pas l’efficacité des œstrogènes.
Tous les œstrogènes sont efficaces, par toutes les voies d’administration : orale (par la bouche), percutanée (gel) et transdermique (patch).
Les phytoestrogènes sont des substances naturelles d’origine végétale (soja) : s’ils semblent efficaces sur la diminution des bouffées de chaleur, leur action sur l’os n’a absolument pas été démontrée.
Les doses minimales d’œstrogènes nécessaires pour freiner la perte osseuse post-ménopausique, en fonction du type de molécule et de leur voie d’administration, ont été définies sur la base d’études prospectives contrôlées, méthodologiquement correctes. Toutefois, la dose efficace est variable selon l’individu.
La durée du traitement
La durée optimale de traitement est l’interrogation majeure. L’effet protecteur des œstrogènes disparaît lorsque l’on arrête le traitement. Certains proposent de prolonger le traitement au moins 10 à 15 ans, pour protéger le plus tard possible, ce qui pose le problème des risques du traitement. D’autres conseillent de mettre en route le THS plus tard, après 65 ans, ce qui prive des autres bénéfices du THS à la ménopause (en particulier sur les bouffées de chaleur).
Une troisième voie a été suggérée : une première séquence, à partir de la ménopause, et pendant 5 à 7 ans, préviendrait l’ostéoporose au poignet et au niveau vertébral, et améliorerait les manifestations fonctionnelles, sans augmenter le risque de cancer du sein ; une deuxième séquence, à partir de 70 ans, pourrait être envisagée chez les femmes ayant le plus de risques de fracture.
La réponse osseuse au THS s’observe à tous les âges, et il n’est jamais trop tard pour débuter un traitement hormonal ; si le traitement est débuté plusieurs années après la ménopause, il faut privilégier le traitement continu pour éviter les règles, et commencer par de petites doses pour éviter les effets secondaires.
Les contre-indications
Il existe des contre-indications au THS :
- cancer du sein et de l’utérus ;
- antécédents de phlébite spontanée avec ou sans embolie pulmonaire ;
- lupus érythémateux disséminé et porphyrie ;
- affection hépatique grave et évolutive.
Les alternatives au THS
Elles peuvent être utiles en cas de contre-indication ou de refus de celui-ci.
Les modulateurs sélectifs des récepteurs aux œstrogènes (SERM) : le chef de file en est le raloxifène qui a fait la démonstration de son effet sur l’os sans effet néfaste sur le sein ni sur l’utérus. Il est actuellement commercialisé en France, mais non remboursé. Malheureusement, en l’absence d’études publiées chez les femmes ayant eu un cancer du sein, il est pour le moment interdit dans ce cas.
Les biphosphonates : l’étidonate n’est autorisé que dans l’ostéoporose post-ménopausique fracturaire avec au moins un tassement vertébral. Il est toutefois également utilisé à titre préventif de l’ostéoporose cortisonique. L’alendronate a obtenu son autorisation de mise sur le marché dans l’ostéoporose post-ménopausique, qu’il y ait des fractures ou non. Toutefois, il n’est remboursé que dans l’ostéoporose fracturaire. D’autres biphosphonates sont à l’étude.
Le fluor et la calcitonine ne sont actuellement plus utilisés dans le traitement de l’ostéoporose. Toutefois la calcitonine reste utile à titre antalgique pendant la phase aiguë du tassement vertébral.
Les mesures hygiéno-diététiques
Celles-ci sont à respecter tout au long de la vie. Il faut prévenir la carence en calcium et en vitamine D, supprimer alcool, tabac, café, faire de l’exercice physique, éviter les chutes, en améliorant la vue, en aménageant le domicile, en limitant les médicaments diminuant la vigilance.
Vos questions
Qu’est-ce que l’ostéoporose ?
L’ostéoporose est une maladie du squelette, associant une diminution de la densité des os et des altérations de la micro-architecture osseuse. Elle provoque une augmentation de la fragilité osseuse, avec accroissement du risque de fracture. On peut en faire le diagnostic grâce à la densitométrie osseuse. L’Organisation mondiale de la santé (OMS) a donné une définition densitométrique de l’ostéoporose : on parle d’ostéoporose si la densité osseuse est inférieure à un seuil défini.
Quand penser à l’ostéoporose ?
Il faut penser à l’ostéoporose :
- au moment de la ménopause, si la femme a d’autres facteurs de risque d’ostéoporose : antécédents familiaux d’ostéoporose, petit gabarit, tabagisme, antécédents d’hyperthyroïdie ou de traitement corticoïde, faible ration calcique.
- après 75 ans chez le sujet âgé, souvent carencé en calcium et vitamine D, ayant une activité physique réduite, avec un risque important de chute.
- en cas de fracture pour un traumatisme minime : fracture du poignet, tassement vertébral, fracture du col du fémur.
- en cas de perte de taille importante, de douleurs ou de déformations de la colonne vertébrale.
- en cas de maladie ou de traitement favorisant l’ostéoporose.
L’ostéoporose est-elle douloureuse ?
Non, l’ostéoporose n’est pas douloureuse, sauf en cas de fracture : c’est une « menace silencieuse ». La douleur apparaît au moment de la fracture : poignet, vertèbres, col du fémur.
Le tassement vertébral peut être à l’origine d’une douleur aiguë, mais il peut être aussi très peu douloureux et faire évoquer des douleurs en rapport avec une simple arthrose. A la longue, les tassements vertébraux peuvent entraîner des déformations de la colonne à l’origine de douleurs chroniques, avec un retentissement sur la qualité de vie.
Est-il normal de se tasser ?
Non. Il est normal de perdre 2 à 3 cm au total, progressivement, avec les années. Une diminution excessive de la taille doit faire rechercher une anomalie de la colonne vertébrale : aggravation des défauts de courbure de la colonne (scoliose, cyphose dorsale et lordose lombaire) ; pincements discaux multiples ; tassements vertébraux.
Y a-t-il un rapport entre ostéoporose et arthrose ?
Schématiquement, l’ostéoporose et l’arthrose sont deux maladies bien différentes. L’ostéoporose est une maladie de l’os, l’arthrose est une maladie de l’articulation. Ces deux maladies ont des facteurs de risques très différents : l’obésité favorise l’arthrose, alors que la maigreur favorise l’ostéoporose…
En fait, ces deux maladies peuvent tout à fait coexister chez la même personne : les tassements vertébraux entraînent à la longue des déformations de la colonne, et peuvent ainsi favoriser ou aggraver une arthrose vertébrale.
Doit-on suivre un régime alimentaire pour l’ostéoporose ?
Oui, l’alimentation joue un rôle important dans l’acquisition et le maintien de la masse osseuse. Il faut manger suffisamment de calcium : produits laitiers, certaines eaux minérales. Le lait de soja étant plus pauvre en calcium que le lait de vache, il faut donc qu’il soit enrichi en calcium.
Il ne faut pas abuser du sel ni des protéines animales (viande, poisson, œufs). Il faut éviter le tabac, l’alcool, le café.
Le calcium fait-il grossir ?
Non, le calcium en soi n’apporte pas de calories et ne favorise donc pas la prise de poids. En revanche, la plupart des aliments riches en calcium sont également riches en graisses : fromages… Si l’on veut éviter une prise de poids ou suivre un régime contre le cholestérol, il faut consommer des produits laitiers allégés : la quantité de calcium est conservée.
Pourquoi le traitement hormonal substitutif est-il le principal traitement de l’ostéoporose ?
La ménopause est la principale cause d’ostéoporose, en raison de la carence en œstrogènes qu’elle entraîne. Le traitement hormonal substitutif permet de compenser cette carence, et donc d’atténuer cette perte osseuse. Mais l’ostéoporose est une maladie « silencieuse », qui ne fait parler d’elle qu’en cas de fracture : l’effet du traitement ne sera donc pas sensible comme l’effet manifeste sur les bouffées de chaleur.
Quel que soit l’âge, le traitement hormonal substitutif est efficace pour freiner la perte osseuse : il n’est donc jamais trop tard pour l’instaurer. Le traitement associe en général aux œstrogènes un progestatif, sauf en cas d’hystérectomie (ablation chirurgicale de l’utérus).
Quels sont les risques du traitement hormonal substitutif ?
Des incidents peuvent survenir dans 5 à 10 % des cas : règles trop abondantes, gonflement douloureux des seins, jambes lourdes, œdèmes ou prise de poids. Ces problèmes sont en général dus à une difficulté pour équilibrer les doses. Le traitement doit donc être personnalisé.
Le risque de phlébite est augmenté, surtout au début du traitement : attention à l’association avec le tabac ! Les œstrogènes entraînent un épaississement de la muqueuse utérine : il est donc nécessaire d’associer un progestatif pour limiter cet effet.
Il existe une augmentation modérée du risque de cancer du sein chez la femme traitée par rapport à la femme non traitée : il passe de 45 à 47 cas pour 1 000 après 5 ans de traitement ; il passe de 45 à 51 cas pour 1 000 après 10 ans de traitement.
Le traitement hormonal substitutif fait-il grossir ?
Le traitement hormonal substitutif ne fait grossir que s’il est mal dosé : s’il est bien équilibré, il prévient la prise de poids observée à la ménopause. Il n’y a pas de traitement standard : le traitement doit être adapté à chaque femme. Il est essentiel d’y associer une bonne hygiène de vie alimentaire et physique.
Ostéoporose et ménopause
L’ostéoporose post-ménopausique constitue un problème majeur de santé publique, puisque parmi 100 femmes atteignant actuellement l’âge de la ménopause, 40 souffriront avant la fin de leur existence d’une fracture par fragilité osseuse : fracture du poignet, tassement vertébral, fracture du col du fémur.
Chaque année, en France, on recense 35 000 nouvelles fractures du poignet, 60 000 nouveaux tassements vertébraux et 50 000 nouvelles fractures de l’extrémité supérieure du fémur.
Au cours de la vie, la masse osseuse évolue en 3 phases :
- une phase d’acquisition du capital osseux jusqu’à 20 ans ;
- une phase en plateau de 10 à 30 ans ;
- une phase de perte osseuse, d’abord lente jusqu’à la ménopause, s’accélérant après celle-ci, en raison du déficit œstrogénique.
Les principales conséquences de l’ostéoporose
La diminution de la masse osseuse après la ménopause entraîne une augmentation du risque de fracture.
- La première fracture d’ostéoporose est la fracture du poignet, dont la fréquence s’élève rapidement dans les 5 années qui suivent la ménopause, pour atteindre un maximum vers 55-60 ans.
- Le tassement vertébral survient aux alentours de 65-70 ans. Il se traduit le plus souvent par une lombalgie aiguë : tout lumbago après 60 ans doit faire suspecter un tassement vertébral et impose des radiographies. Il peut être asymptomatique, se traduisant simplement par une diminution de la taille.
- La fracture du col du fémur survient aux alentours de 75-80 ans : elle est grave chez le sujet âgé, et est à l’origine du décès dans l’année qui suit la fracture dans 20 % des cas.
La survenue d’une fracture du poignet, d’un tassement vertébral ou d’une fracture du col du fémur après la ménopause impose la densitométrie osseuse pour confirmer le diagnostic d’ostéoporose avant de débuter un traitement.
La prévention des fractures
Toutefois, il est aujourd’hui possible de faire le constat d’une fragilité osseuse avant la facture :
- Grâce au dépistage des femmes à risque : femme blanche ou asiatique ; de petit gabarit ; avec des antécédents familiaux d’ostéoporose ; ayant eu une puberté tardive, une ménopause précoce ; ayant un régime pauvre en produits laitiers ; avec une consommation exagérée de tabac, d’alcool et de café ; ayant peu d’activité physique ; avec des antécédents de corticothérapie prolongée, d’hyperthyroïdie…
- Par la densitométrie osseuse, afin de confirmer le diagnostic.
La constatation d’une ostéoporose, qu’elle soit fracturaire ou non, doit conduire à une prise en charge thérapeutique ou préventive. La prévention de l’ostéoporose peut s’appliquer à tous les âges de la vie :
- En optimisant le pic de masse osseuse : par une ration calcique suffisante et grâce à un exercice physique adapté ;
- En ralentissant la perte osseuse par carence œstrogénique après la ménopause, grâce à un traitement hormonal substitutif ;
- En ralentissant la perte osseuse chez le sujet âgé, par la correction de la carence en calcium et vitamine D ;
- A tout âge, en respectant certaines règles hygiéno-diététiques : outre l’exercice physique, l’apport suffisant en calcium et/ou vitamine D, il faut éviter certains toxiques comme l’alcool, le tabac, le café.
Ostéoporose masculine
Bien que moins fréquente que chez la femme, l’ostéoporose masculine n’est pas une maladie rare : plusieurs études épidémiologiques ont montré que 6 à 8 % des hommes auront une fracture ostéoporotique dans leur vie.
Chez la femme, la carence en hormones sexuelles après la ménopause explique l’accroissement de la perte osseuse entraînant une fragilité osseuse. Chez l’homme, il n’existe pas de véritable andropause et la diminution de la testostéronémie est progressive et modérée : le facteur hormonal intervient donc peu dans la genèse de l’ostéoporose masculine. En revanche, la perte osseuse après 70 ans est la même que chez la femme. Une cause peut être retrouvée dans près de la moitié des cas.
Le diagnostic
Le diagnostic se fait le plus souvent devant un tassement vertébral, parfois devant une fracture survenant pour un traumatisme minime. Le diagnostic est densitométrique, mais la définition de l’ostéoporose densitométrique de la femme n’est en principe pas applicable à l’homme.
Chez l’homme, il est nécessaire de rechercher une étiologie à traiter éventuellement, même si, dans la moitié des cas, on ne trouve pas de cause particulière à l’ostéoporose masculine :
- une maladie endocrinienne : hyperthyroïdie, hyperparathyroïdie, déficit en testostérone (attention à l’adénome hypophysaire à prolactine), hypercorticime, dû à une maladie de Cushing (hyperfonctionnement de la corticosurrénale) ou le plus souvent à un traitement par les corticoïdes ;
- une anomalie rénale : hypercalciurie, qu’il faut savoir détecter car elle peut être aggravée par l’administration intempestive de calcium et vitamine D ; diabète phosphoré (fuite rénale de phosphore) ; acidose tubulaire ;
- une maladie digestive chronique, intestinale ou hépatique ;
- certaines maladies rares : maladie de Lobstein (ostéogenèse imparfaite, héréditaire) ; hémochromatose ; mastocytose.
Comme chez la femme, il faut rechercher certains facteurs de risques : diminution des apports calciques, consommation d’alcool, de tabac, de café, sédentarité. La composante génétique est également importante.
Le traitement
C’est d’abord celui de la cause : traitement par testostérone d’un hypogonadisme (après avoir éliminé un adénome à prolactine). En cas de corticothérapie prolongée, il faut prescrire la dose minimale efficace de corticoïdes ; un traitement par calcium et vitamine D est utile ; l’utilisation des biphosphonates sous la forme d’étidronate est autorisée.
Le sevrage de l’alcool et du tabac est difficile et doit s’inscrire dans une démarche nutritionnelle globale.
Dans l’hypercalciurie, la limitation de la consommation de sel et de viande (qui favorise la fuite rénale de calcium) suffit parfois. Si elle persiste, on peut adjoindre des diurétiques thiazidiques.
Les autres moyens thérapeutiques sont limités :
- L’exercice physique peut apporter un bénéfice.
- La supplémentation en calcium et vitamine D est plus efficace chez le sujet âgé (souvent carencé) que chez l’homme jeune. Elle peut être intéressante chez l’alcoolique et au cours des maladies digestives chroniques.
- Les biphosphonates utilisés chez la femme ménopausée n’ont pas été étudiés chez l’homme : ils n’ont donc pas l’autorisation de mise sur le marché dans l’ostéoporose masculine, et ne peuvent donc pas être prescrits.
Il faut insister sur la prévention du risque de chute : améliorer la vue, aménager le domicile, diminuer certains médicaments qui diminuent la vigilance (somnifères, tranquillisants).